Laboratorio # 1
Alcohol absoluto
Objetivo.-
Deshidratar alcohol comercial para obtener alcohol absoluto por el método de separación por destilación.
Fundamento teórico.-
La destilación del alcohol comercial siempre tiene una composición aproximada de 95% de alcohol y 5% de agua, como si fuera un líquido puro, esa mezcla forma un AZEÓTROPO con un punto de ebullición constante.
Para deshidratar el alcohol usaremos benceno que destila formando una mezcla azeotrópica compuesta de alcohol etílico.
P1= 18.5% de alcohol etílico
P2= 74.1% de benceno
P3= 7.4% de agua
Con un punto de ebullición mínimo de 64.9oC
(H2OCH3 – CH2OH)n + C6H6 = C6H6(H2O)n + CH3 – CH2OH
Etanol Benceno alcohol absoluto
El alcohol absoluto se lo obtiene por destilación de la mezcla Alcohol-Agua-Benceno, después hay una mezcla alcohol-benceno que destila a 68.24oC, y finalmente se suspende la destilación alrededor de 76oC.
El alcohol absoluto se lo utiliza como combustible de motores, en cosmética, en análisis químico, etc.
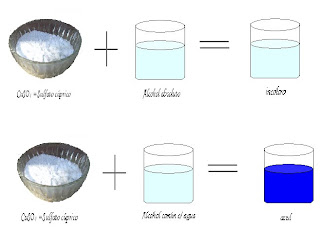
El alcohol absoluto se comprueba con sulfato de cobre anhidro que es un sólido blanco el que se AZULEA si el alcohol tiene agua.
SO4Cu + 5H2O = SO4Cu.5H2O (1)
Blanco azul
Si el alcohol tiene agua le comunica turbidez a los hidrocarburos.
Arde con llama azul, casi incolora cuando es puro.
CH3 – CH2OH + 3O2 = 2CO2 + 3H2O (2)
Para la experiencia, las relaciones en volúmenes de alcohol comercial y benceno V, V2, serán:
V= 100 P3 (3) V2= P2 (4)
P 2
Relacionando 3 y 4
V = 100 P3 2 = C = Constante (5)
V2 P2
La relación de volumen de alcohol respecto al volumen de benceno es una constante “C”, para cualquier otro volumen de ambos se cumple la ecuación (5).
Donde:
P = 5 gr. o ml. que es el porcentaje de agua del alcohol común.
= 0.789 gr. / cc. Que es la densidad del alcohol comercial.
2 = 0.879 gr. / cc. Que es la densidad del benceno
Para:
V2 = 60 ml. de benceno, se necesitan según la ecuación (5)
V = 134 ml. de alcohol común, usaremos 130 ml.
Técnica operativa.-
Materiales.-
1 Equipo de destilación
1 Termómetro de 100 oC
1 Mechero
1 Puñado de granallas
1 Soporte con agarraderas
1 Trípode con malla
4 Beakers de 100 ml. y 50 ml.
2 Probetas de 100 ml. y 200 ml.
130 ml de alcohol común
60 ml. de benceno
20 gr. de sulfato de cobre anhidro
50 ml. de gasolina
1 caja de fósforo
Esquema.-
Alcohol absoluto
Objetivo.-
Deshidratar alcohol comercial para obtener alcohol absoluto por el método de separación por destilación.
Fundamento teórico.-
La destilación del alcohol comercial siempre tiene una composición aproximada de 95% de alcohol y 5% de agua, como si fuera un líquido puro, esa mezcla forma un AZEÓTROPO con un punto de ebullición constante.
Para deshidratar el alcohol usaremos benceno que destila formando una mezcla azeotrópica compuesta de alcohol etílico.
P1= 18.5% de alcohol etílico
P2= 74.1% de benceno
P3= 7.4% de agua
Con un punto de ebullición mínimo de 64.9oC
(H2OCH3 – CH2OH)n + C6H6 = C6H6(H2O)n + CH3 – CH2OH
Etanol Benceno alcohol absoluto
El alcohol absoluto se lo obtiene por destilación de la mezcla Alcohol-Agua-Benceno, después hay una mezcla alcohol-benceno que destila a 68.24oC, y finalmente se suspende la destilación alrededor de 76oC.
El alcohol absoluto se lo utiliza como combustible de motores, en cosmética, en análisis químico, etc.
El alcohol absoluto se comprueba con sulfato de cobre anhidro que es un sólido blanco el que se AZULEA si el alcohol tiene agua.
SO4Cu + 5H2O = SO4Cu.5H2O (1)
Blanco azul
Si el alcohol tiene agua le comunica turbidez a los hidrocarburos.
Arde con llama azul, casi incolora cuando es puro.
CH3 – CH2OH + 3O2 = 2CO2 + 3H2O (2)
Para la experiencia, las relaciones en volúmenes de alcohol comercial y benceno V, V2, serán:
V= 100 P3 (3) V2= P2 (4)
P 2
Relacionando 3 y 4
V = 100 P3 2 = C = Constante (5)
V2 P2
La relación de volumen de alcohol respecto al volumen de benceno es una constante “C”, para cualquier otro volumen de ambos se cumple la ecuación (5).
Donde:
P = 5 gr. o ml. que es el porcentaje de agua del alcohol común.
= 0.789 gr. / cc. Que es la densidad del alcohol comercial.
2 = 0.879 gr. / cc. Que es la densidad del benceno
Para:
V2 = 60 ml. de benceno, se necesitan según la ecuación (5)
V = 134 ml. de alcohol común, usaremos 130 ml.
Técnica operativa.-
Materiales.-
1 Equipo de destilación
1 Termómetro de 100 oC
1 Mechero
1 Puñado de granallas
1 Soporte con agarraderas
1 Trípode con malla
4 Beakers de 100 ml. y 50 ml.
2 Probetas de 100 ml. y 200 ml.
130 ml de alcohol común
60 ml. de benceno
20 gr. de sulfato de cobre anhidro
50 ml. de gasolina
1 caja de fósforo
Esquema.-

Como siempre primero se limpia el equipo de destilación, se colocan las granallas, las cantidades indicadas de alcohol y benceno y se procede a la destilación con llama moderada,
 Empieza a destilar a 38 oC,
Empieza a destilar a 38 oC,Se para la destilación a una temperatura de 75 oC
Se comprueban las propiedades de turbidez y combustión del alcohol absoluto y del destilado.
Cálculos.-
Se determina la cantidad de destilado V en ml. y se lo compara con V2, seguidamente se determina la cantidad que queda de alcohol absoluto en el balón de destilación V en ml. y el rendimiento porcentual “n”.
n = v * 100
V
Para el alcohol común:
Por cada 100 gr. de alcohol común 5 gr. son de agua
“X” gr. de alcohol común voy a necesitar Para 7.4 gr. de agua
X = 100 gr. * 7.4 gr.
5 gr.
X = 148 gr. de alcohol común
187.5 ml. de alcohol común
Si 0.789 gr. mide 1 ml.
Entonces 148 gr. mide “X” ml.
X = 1 ml * 148 gr.
0.789 gr.
X = 187.5 ml. de alcohol común
Para el benceno:
Si 0.879 gr. de benceno mide 1 ml
Entonces 74.1 gr. de benceno mide “X” ml.
X = 1 ml. * 74.1 gr. de benceno 84.3 ml. de benceno
0.879 gr. de benceno
X = 84.3 ml. de benceno
Para el alcohol absoluto:
Si 95 gr. de alcohol abs. Se mezclan con 5 gr. de agua
“X” gr. de alcohol abs. Voy a necesitar 7.4 gr. de agua
X = 95 gr. * 7.4 gr.
5gr.
X = 140 gr. de alcohol absoluto
Para la constante:
V1 P3 * 2 * 100 “C”
V2 P * * P2
C = 7.4 * 0.879 * 100
5 * 0.789 * 74.1
C = 2.225
Se determina la cantidad de destilado V en ml. y se lo compara con V2, seguidamente se determina la cantidad que queda de alcohol absoluto en el balón de destilación V en ml. y el rendimiento porcentual “n”.
n = v * 100
V
Para el alcohol común:
Por cada 100 gr. de alcohol común 5 gr. son de agua
“X” gr. de alcohol común voy a necesitar Para 7.4 gr. de agua
X = 100 gr. * 7.4 gr.
5 gr.
X = 148 gr. de alcohol común
187.5 ml. de alcohol común
Si 0.789 gr. mide 1 ml.
Entonces 148 gr. mide “X” ml.
X = 1 ml * 148 gr.
0.789 gr.
X = 187.5 ml. de alcohol común
Para el benceno:
Si 0.879 gr. de benceno mide 1 ml
Entonces 74.1 gr. de benceno mide “X” ml.
X = 1 ml. * 74.1 gr. de benceno 84.3 ml. de benceno
0.879 gr. de benceno
X = 84.3 ml. de benceno
Para el alcohol absoluto:
Si 95 gr. de alcohol abs. Se mezclan con 5 gr. de agua
“X” gr. de alcohol abs. Voy a necesitar 7.4 gr. de agua
X = 95 gr. * 7.4 gr.
5gr.
X = 140 gr. de alcohol absoluto
Para la constante:
V1 P3 * 2 * 100 “C”
V2 P * * P2
C = 7.4 * 0.879 * 100
5 * 0.789 * 74.1
C = 2.225
Conclusiones.-
Se ha obtenido el alcohol absoluto por destilación del alcohol común y al final se ha comparado si efectivamente era alcohol absoluto o no. A nuestro alcohol absoluto se la agrego unos gramos de sulfato cúprico y hemos obtenido una solución incolora, y esto efectivamente comprueba que si es verdadero absoluto.
Se ha obtenido el alcohol absoluto por destilación del alcohol común y al final se ha comparado si efectivamente era alcohol absoluto o no. A nuestro alcohol absoluto se la agrego unos gramos de sulfato cúprico y hemos obtenido una solución incolora, y esto efectivamente comprueba que si es verdadero absoluto.
video
No hay comentarios:
Publicar un comentario